贝美替尼
货号:
IB2430
品牌:
Jinpan
暂无详情
产品简介
| 有效期 | 2年 |
| 别名 | MEK-162;ARRY-162;ARRY-438162;比尼替尼 |
| 英文名称 | Binimetinib |
| CAS | 606143-89-9 |
| 分子式 | C17H15BrF2N4O3 |
| 分子量 | 441.23 |
| 储存条件 | 2-8℃ |
| 纯度 | ≥98% |
| 外观(性状) | White to off-white (Solid) |
| 单位 | 瓶 |
| 生物活性 | Binimetinib (MEK162) 是口服和选择性的 MEK1/2 抑制剂,IC50 为12 nM。[1-5] |
| In Vitro | 在MCF7细胞中,RSK3或RSK4表达降低了对单独使用任何PI3K抑制剂治疗的反应。然而,PI3K抑制与Binimetinib(MEK162)或BI-D1870的组合完全逆转了表达RSK的细胞的抗性[2]。 Binimetinib(MEK162)阻断所有HRAS突变细胞系中的基础ERK磷酸化。依维莫司和AZD6244 / MEK162的组合比在Western印迹上单次使用依维莫司更能抑制S6激酶。依维莫司和AZD6244 / MEK162的组合也转化为HRAS突变细胞中比单次使用更强的细胞生长阻断。 Binimetinib(MEK162)与依维莫司的协同作用强于AZD6244 [3]。 |
| In Vivo | 在两种动物模型中,用Binimetinib(ARRY-438162)治疗以剂量相关的方式降低疾病严重性。 CIA模型中的ARRY-438162在1和3mg / kg时抑制踝部直径增加27%和50%,而布洛芬具有46%的抑制。当与布洛芬组合时,这两个相同的剂量分别导致74%和72%的抑制。踝关节的显微镜检查显示,Binimetinib(ARRY-438162)在1和3 mg / kg时显着抑制病变(炎症,软骨损伤,血管pan形成和骨吸收)32%和60%,而单独使用布洛芬治疗则导致17 %抑制,与对照无显着差异。当这两剂Binimetinib(ARRY-438162)与布洛芬联合使用时,对关节破坏的抑制率为54%和77%。在AIA中,3和10mg / kg的Binimetinib(ARRY-438162)抑制AIA踝关节直径11%和34%,而MTX具有33%的抑制。当与MTX组合时,3和10mg / kg的Binimetinib(ARRY-438162)导致55%和71%的抑制。用于炎症和骨吸收的踝关节的显微镜检查也显示出与单独的化合物相比改善的功效[1]。当Binimetinib(MEK162)与BEZ235组合时,观察到肿瘤生长显着减少(P = 0.01)。抗肿瘤活性的这种增加伴随着磷酸-ERK和磷酸-S6染色的减少。在磷酸化4EBP1染色中没有观察到显着变化,磷酸化4EBP1染色是mTOR活性的直接靶标[2]。 |
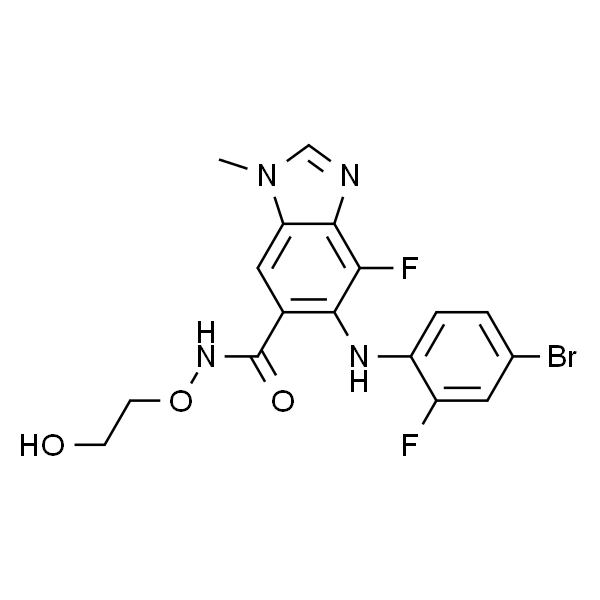
| SMILES | BrC1=CC=C(C(F)=C1)NC2=C(C3=C(C=C2C(NOCCO)=O)N(C=N3)C)F |
| 靶点 | MEK |
| 动物实验 | 小鼠[2]六周龄雌性无胸腺裸鼠Foxn1nu小鼠购自Harlan Laboratories。将小鼠置于空气过滤的层流柜中,12小时光照/ 12小时黑暗循环,随意给予食物和水。用无菌操作处理小鼠并使其在实验操作前适应当地条件1周。在细胞注射前1天将17β-雌二醇颗粒皮下植入每只小鼠。将107个MCF-GFP或MCF7-RSK4细胞重悬于PBS / Matrigel(1:1)中,并以200μL终体积皮下注射到每只小鼠的右胁腹中。当肿瘤达到250mm 3的平均尺寸时开始治疗,因此被认为是已建立的生长异种移植物。通过口服强饲法每天一次用安慰剂,BEZ235,BKM120,MK-2206或Binimetinib(MEK162)处理小鼠。将BEZ235(25-30mg / kg,6IW [1天休息6天])和BKM120(30mg / kg,6IW)溶解于新配制的10%NMP-90%PEG中,并在30分钟内给药。将MK-2206(100mg / kg,3IW)配制在0.5%吐温-80,1%羧甲基纤维素中的30%Captisol和Binimetinib(MEK162)(6mg / kg,BID)中。对于肿瘤生长研究,根据异种移植模型和治疗方案,将小鼠治疗7-24天。用卡尺每周测量3次肿瘤异种移植物,并使用下式确定肿瘤体积:(长×宽2)×(π/ 6)。在实验结束时,用1.5%异氟醚 – 空气混合物麻醉动物并通过颈脱位法杀死。最后一次给药后2小时取出肿瘤。大鼠[1]大鼠胶原诱导的关节炎(CIA)和大鼠佐剂诱导的关节炎(AIA)模型用于确定亚急性炎症环境中的功效。在CIA研究中,通过注射II型胶原诱导的已确定疾病的大鼠用0.3,1或3mg / kg ARRY-438162(PO,BID)治疗,有或没有30mg / kg布洛芬(PO,QD)六天。体重和踝直径用于监测第0-7天的疾病进展。在第0天通过在FCA中注射类脂胺诱导AIA模型。从第8天开始用1或3mg / kg双甲基替尼(ARRY-438162)(PO,QD)处理AIA大鼠并继续6天,加入或不加入0.05mg / kg甲氨蝶呤(PO,QD),其在0-13天给药。在第7-14天监测疾病进展,测量爪子直径和体重。 |
| 细胞实验 | 如图所示感染的MCF7细胞接种在12孔板(2×104)中。 24小时后,用BEZ235(100或200 nM),BKM120(0.75或1μM),GDC-0941(1μM)或MK2206(2μM)单独或与Binimetinib(MEK162)(1μM)联合处理细胞),BI-D1870(10μM)或AZD6244(1μM),如文中所示。通过用4%戊二醛或甲醇固定细胞,在H 2 O中洗涤细胞两次,并用0.1%结晶紫染色细胞来定量细胞数。随后用10%乙酸萃取染料,测定其吸光度(570nm)。生长曲线一式三份进行。使用CellTiter-Glo的活力测定通过在96孔板中铺板2,000个细胞,在24小时时添加药物,并在添加药物后4至5天进行测定来进行。通过流式细胞术定量细胞周期和亚二倍体凋亡细胞。简而言之,用PBS洗涤细胞,在冷的70%乙醇中固定,然后用RNA酶处理碘化丙锭染色。使用Cell Quest软件在FACScalibur细胞计数器中进行亚G1细胞的定量分析[2]。 |
| 数据来源文献 | [1]. J Pheneger, et al. 2006, ACR Annual Scientific Meeting. Abst 794.
[2]. Serra V, et al. RSK3/4 mediate resistance to PI3K pathway inhibitors in breast cancer. J Clin Invest, 2013, 123(6), 2551-2563. [3]. Kiessling MK, et al. Mutant HRAS as novel target for MEK and mTOR inhibitors. Oncotarget. 2015 Dec 8;6(39):42183-96. [4]. Cheng H, et al. PIK3CA(H1047R)- and Her2-initiated mammary tumors escape PI3K dependency by compensatory activation of MEK-ERK signaling. Oncogene. 2016 Jun 9;35(23):2961-70. [5]. Seip K, et al. Fibroblast-induced switching to the mesenchymal-like phenotype and PI3K/mTOR signaling protects melanoma cells from BRAF inhibitors. Oncotarget. 2016 Apr 12;7(15):19997-20015 |
| 规格 | 5mg 10mg |
是选择性的 MEK1/2 抑制剂。
