蓝色-琼脂糖凝胶6FF
| 有效期 | 1年 |
| 英文名称 | Sepharose 6FF |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 25ml 100ml |

蓝色-琼脂糖凝胶6FF
| 有效期 | 1年 |
| 英文名称 | Sepharose 6FF |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 25ml 100ml |
琼脂糖凝胶4FF
| 有效期 | 5年 |
| 英文名称 | Sepharose 4FF |
| 储存条件 | 2-8℃ |
| 外观(性状) | 颗粒 |
| 单位 | 瓶 |
| 规格 | 100ml |
产品简介:
琼脂糖凝胶4FF是在琼脂糖凝胶4B的基础上经过两次交联形成的高交联基质,微球的化学稳定性及物理性能显著增强,刚性增加,流速更快,使产品处理时间大大缩短。可用于生物大分子的凝胶层析。
1. 外观
本品为白色球状凝胶,无嗅、无味、无肉眼可见杂质。
2. 理化指标
|
项 目 |
指 标 |
|
基 质 |
4% 交联琼脂糖 |
|
排阻极限 |
6×104~2×107 (球蛋白) |
|
形状 |
球形 |
|
粒径 |
45~165 μm |
|
最高流速 |
300 cm/h* |
|
耐压 |
0.30 MPa |
|
pH适用范围 |
2~14 (短时间,在位清洗),2~12(长时间) |
|
化学稳定性 |
以下溶液中40℃下稳定: 2mol/L NaOH;70%EtOH;30%异丙醇;30%乙腈;1%SDS;6mol/L盐酸胍;8mol/L尿素 |
*检测条件: 层析柱10mm×300mm *柱床高15cm,25℃, 流动相为0.1mol/LNaCl
3. 贮存
产品应密封贮存在4℃~25℃(保存溶液为20% 乙醇),通风、干燥、清洁的地方。不能冷冻。用过的柱子贮存在4℃(20% 乙醇)。
4. 注意事项
本品应避免与氧化剂接触,避免长时间暴露在空气中。运输中应避免日晒、雨淋、重压,严禁与有毒、有害物品混运。
5. 应用
本产品具有很高的化学稳定性、高流速、较好的机械性能、可多次重复使用等特点,非特异性吸附低,回收率高,可用有机溶剂及1~2mol/L 的NaOH在位清洗,适用于工业规模生产,广泛用于生物制药和生物工程下游蛋白质、核酸及多肽的凝胶色谱纯化。
5.1 装柱
凝胶过滤介质的使用对装柱的要求较高,为了保证分离效果,一般通过柱子上加一个装柱器来使分离柱装满凝胶,或采用带有轴向加压装置的柱子。凝胶柱床一般高于60cm。装柱效果可用染料或丙酮-水溶液进行检验。以下过程为通用介质装填过程。若为带有轴向加压装置的柱子,可在柱床稳定后将柱床压紧,接好管路。
(1)让所有的材料和试剂达到室温。配制缓冲液。凝胶层析上样、平衡和洗脱只用一种低盐浓度的缓冲液。
(2)选择一根一定直径的柱子,长约30~60cm,根据柱子大小取所需量的凝胶(约为柱床体积的1.15倍),清洗掉20%乙醇,抽干,用缓冲液(按凝胶:缓冲液=3:1的比例)配成匀浆。
(3)将柱内及柱子底端用水或缓冲液润湿并保持一小段液位(液面略高于滤膜),务必使底端无气泡。
(4)用玻璃棒引导匀浆沿着柱内壁一次性倒入柱内,注意勿使产生气泡。打开柱子出液口,使凝胶在柱内自由沉降,连结好柱子顶端柱头。
(5)打开蠕动泵,让缓冲液用使用时流速的1.33倍的流速流过,使柱床稳定。用缓冲液平衡柱子,到柱床稳定。
(6)最好用一个装柱器辅助装柱。装完后柱床上端轻轻刮平,上好柱头。
5.2 平衡
让缓冲液以一定流速流过柱子,到流出液电导和pH不变。
5.3 上样
(1)样品用缓冲液配制,浑浊的样品要离心和过滤后上样。含盐量过大、浓度过小的样品要先做处理,再上样。
(2)介质对样品组分的分离是按组分分子量大小进行的,分子量大的先流出来。
(3)上样体积约为柱体积的1~2%,越小分离越好。
5.4 洗脱
用缓冲液洗脱,洗脱中保持流速、缓冲液组成不变。
5.5 再生
一般用缓冲液洗到平衡,可再次使用。
5.6 注意
在装柱、使用和保存柱子的时候,始终要避免柱子流干气泡进入。若有失活蛋白质或脂类物质在再生时洗不掉,可用在位清洗(CIP)除去。
5.7 在位清洗
(1)对于以离子键结合上去的蛋白,可以用2M NaCl去除。
(2)对沉淀蛋白、对以疏水性结合的蛋白或脂类,可用1M NaOH 去除。
(3)对强疏水性结合的蛋白、脂类等,用4~10倍柱体积的70%乙醇或30%异丙醇清洗,但要注意有机溶剂的浓度以梯度的方式逐渐增加,否则容易产生气泡。
清洗完毕后,用至少3倍缓冲液平衡柱子。
5.8 注意
在装柱、使用和保存柱子的时候,要避免柱子流干气泡进入。
5.9 去热源
用0.5M的氢氧化钠清洗柱子5~6小时或用0.1M的氢氧化钠24小时。或用以下方法步骤去除:
(1)2倍柱体积的70%乙醇;
(2)2倍柱体积50mM Tris-HCl pH7.5;
(3)1倍柱体积4M尿素;
(4)3倍柱体积的Tris缓冲液+0.1M Nacl;
以上缓冲液都在无热源的双蒸水中配制。
5.10 消毒
用0.5~1M NaOH室温下洗8~10倍柱体积,初始缓冲液平衡柱子。
注意:上样之前,样品必须去除色素,否则色素会被吸附到填料上,影响填料的正常使用。
备注:产品信息可能会有优化升级。请以实际标签信息为准。
Q-琼脂糖凝胶FF
| 有效期 | 3年 |
| 别名 | 快流速Q琼脂糖凝胶 |
| 英文名称 | Q-Sepharose Fast Flow |
| 储存条件 | 2-8℃ |
| 外观(性状) | 本品为白色球状凝胶,无嗅、无味、无肉眼可见杂质。 |
| 单位 | 瓶 |
| 规格 | 100ml |
一、简介
Q-琼脂糖凝胶FF是将三甲胺基烷基季铵基团键合在高流速琼脂糖微球上形成的一种强阴离子交换介质。广泛用于生物制药和生物工程下游蛋白质、核酸及多肽的离子交换制备。
本品为白色球状凝胶,无嗅、无味、无肉眼可见杂质。
二、亲和填料特性
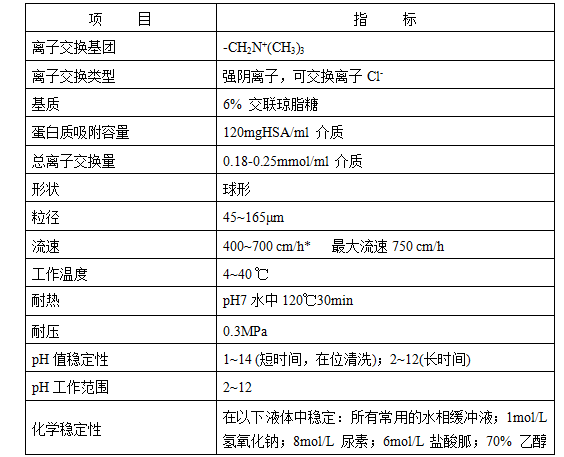
*检测条件: 层析柱10mm×300mm *柱床高15cm,25℃,流动相为0.1mol/LNaCl。.
三、 适用范围
本产品具有高化学稳定性、高流速、高载量、好的机械性能、可在位清洗、多次重复使用等特点,非特异性吸附低,回收率高,适用于工业规模生产,适用于在pH工作范围内可形成负离子的生物大分子的分离纯化,广泛用于生物制药和生物工程下游蛋白质、核酸及多肽的离子交换制备。
四、操作说明
1 装柱
(1)让所有的材料和试剂达到室温。配制初始缓冲液(平衡液)和洗脱缓冲液。
(2)根据柱子大小取所需量的凝胶,清洗掉20%乙醇,抽干,用初始缓冲液(按凝胶:缓冲液=3:1的比例)配成匀浆。
(3)将柱内及柱子底端用水或缓冲液润湿并保持一小段液位(液面略高于滤膜),务必使底端无气泡。
(4)用玻璃棒引导匀浆沿着柱内壁一次性倒入柱内,注意勿使产生气泡。打开柱子出液口,使凝胶在柱内自由沉降,连结好柱子顶端柱头。
(5)打开蠕动泵,让缓冲液用使用时流速的1.33倍的流速流过,使柱床稳定。用2~3倍柱体积的缓冲液平衡柱子。
2 平衡
让平衡缓冲液以一定流速流过柱子,到流出液电导和pH不变。平衡液是低浓度的缓冲溶液,如Tris、PBS等。
3 上样
(1)样品用平衡液配制,浑浊的样品要离心和过滤后上样。盐浓度太大的样品处理后再配。
(2)一般情况是让目标产品结合在柱子上,用平衡液洗去杂质,再选择一种洗脱液洗下目标产品。
(3)介质对样品组分吸附的程度取决于样品的带电性质、流动相的离子强度和pH值。盐浓度小,介质对样品组分吸附较牢。用DEAE介质时,推荐的pH值是小于目标产品等电点1个单位。
4 洗脱
Q琼脂糖凝胶FF介质可用增大盐浓度或减小pH值进行洗脱,常用增大盐浓度的办法洗脱。
5再生
一般用高盐浓度的缓冲液(含1~2mol/L NaCl)洗或减小pH洗10倍以上柱体积,接着用结合蛋白的平衡液洗到平衡,可再次使用。
若有失活蛋白质或脂类物质在再生时洗不掉,可用在位清洗(CIP)除去。
6 在位清洗
(1)对于以离子键结合上去的蛋白,可以用2M NaCl去除。
(2)对沉淀蛋白、对以疏水性结合的蛋白或脂类,可用1M NaOH 去除。
(3)对强疏水性结合的蛋白、脂类等,用4~10倍柱体积的70%乙醇或30%异丙醇清洗,但要注意有机溶剂的浓度以梯度的方式逐渐增加,否则容易产生气泡。
清洗完毕后,用至少3倍缓冲液平衡柱子。
7 注意
在装柱、使用和保存柱子的时候,要避免柱子流干,气泡进入。
在使用过程中,不能使用强酸,如使用酸洗,应使用浓度低于0.1 M的冰醋酸。
8 去热源
用0.5M的氢氧化钠清洗柱子5~6小时或用0.1M的氢氧化钠24小时。或用以下方法步骤去除:
(1)2倍柱体积的70%乙醇;
(2)2倍柱体积50mM Tris-HCl pH7.5;
(3)1倍柱体积4M尿素;
(4)3倍柱体积的Tris缓冲液+0.1M NaCl;
以上缓冲液都在无热源的双蒸水中配制。
9 消毒
用0.5~1M NaOH室温下洗8~10倍柱体积,初始缓冲液平衡柱子。
10 灭菌
置介质于高压灭菌锅中120℃下30分钟。
五、注意事项
产品应密封贮存在4℃~25℃(保存溶液为20% 乙醇),通风、干燥、清洁的地方。不能冷冻。用过的柱子贮存在4℃(20% 乙醇)。避免与氧化剂接触;避免在pH< 4的环境中长时间暴露(一周,20℃)。
备注:产品信息可能会有优化升级。请以实际标签信息为准。
镍-琼脂糖凝胶6FF
| 有效期 | 1年 |
| 别名 | 镍-琼脂糖凝胶 6FF 镍琼脂糖凝胶 镍柱 |
| 英文名称 | Ni Sepharose 6FF |
| 储存条件 | 2-8℃,有效期1年 |
| 规格 | 5ml 10ml 25ml 100ml |
Ni-NTA琼脂糖凝胶6FF是用于纯化6×His标签重组蛋白的一种纯化介质,它是由6%交联的Sepharose耦连了一种四齿螯合剂NTA而得. 它可用于在非变性或变性条件下纯化任何表达系统表达的6×His标签重组蛋白。NTA,含有四个螯合区,较一般的三齿螯合剂能更好的结合Ni2+。6×His可与Ni2+螯合,从而使His标签蛋白结合在Ni-NTA纯化介质上,未结合的蛋白被洗涤下去,结合在介质上的蛋白经过一定浓度的咪唑或低pH缓冲液的温和洗脱下来,从而得到高纯度的目的蛋白。该纯化介质与His标签蛋白具有极高的亲和力,可达5-20 mg/ml。可在非变性和变性条件下纯化任何表达系统所得的His标签蛋白。纯化程序简单,所得的蛋白纯度可高达95%。Ni-NTA可再生4-6次,重复使用。本产品悬浮液为20%乙醇,已螯合Ni2+。
操作方法:
A. 非变性条件下抽提His标签蛋白
1) 准备细胞,接种,诱导表达。收集细胞,置于-70°C或立即进行步骤2操作。
2) 加入1/20细胞生长体积的NTA-0 Buffer和PMSF。PMSF使用的工作浓度为1 mM现用现加。
3) 将细胞悬浮起来,加入溶菌酶,混匀,冰上放置30分钟,超声或匀浆破碎细胞。该步骤冰上操作。
4) 加入10% Triton X-100, 使终浓度为0.05%,充分混匀,冰上放置15分钟。
5) 12000 rpm/min(20,000×g以上),4°C离心15分钟以上。取上清,置于冰上备用或-20°C保存。
6) 将NTA树脂装入合适的层析柱,层析用10倍NTA体积的NTA-0 Buffer洗。
7) 将样品加至NTA层析柱中,流速在15 ml/h左右,收集穿透部分,用SDS/PAGE分析蛋白的结合情况。
8) 层析用5倍NTA体积的NTA-0 Buffer洗,流速控制在30 ml/h左右。
9) 分别用5倍NTA体积的NTA-20、NTA-40、NTA-60、NTA-80、NTA-100、NTA-200、NTA-1000 Buffer洗脱,流速控制在15 ml/h左右,收集洗脱液,每管收集一个NTA体积。
10) 确定目标蛋白质在洗脱液中的分布情况。最为有效的方式是SDS-PAGE分析。也可以用Bradford 蛋白质测定试剂盒,快速确定蛋白质的含量,然后用SDS/PAGE分析蛋白质的分布。
11)纯化的目标蛋白质的保存条件需要根据蛋白质的性质和用途确定。 NTA-0 、20、40、60、80、100、200、1000Buffer分别为浓度20 mM Tris-HCl pH7.9, 0.5 M NaCl, 10% Glycerol,添加0、20、40、60、80、100、200、1000 mM Imidazole。
B.变性条件下从包涵体中纯化His标签蛋白
1) 准备细胞,接种,诱导表达。收集细胞,置于-70°C或立即进行步骤2操作。
2) 加入1/20细胞生长体积的GuNTA-0 Buffer和PMSF。PMSF使用的工作浓度为1 mM现用现加。
3) 将细胞悬浮起来,冰上超声破碎细胞,降低粘稠度。
4) 室温放置30分钟,间或混匀或用磁力搅拌。
5) 12000转/分(20,000×g以上),4°C离心15分钟以上。取上清,置于冰上备用或-20°C保存。
6) 将NTA树脂装入合适的层析柱,层析用10倍NTA体积的GuNTA-0 Buffer洗。
7) 将样品加到NTA层析柱中,流速控制在15 ml/h左右,收集穿透部分,用于SDS/PAGE分析蛋白质的结合情况。
8) 层析用5倍NTA体积的GuNTA-0 Buffer洗,流速控制在30 ml/h左右。
9) 分别用5倍NTA体积GuNTA-20、GuNTA-40,GuNTA-60、GuNTA-100、GuNTA-500洗脱,流速在15 ml/ h左右,收集洗脱液,每管收集一个NTA体积。
10) 确定目标蛋白质在洗脱液中的分布情况。最为有效的方式是SDS/PAGE分析。也可以用Bradford 蛋白质测定试剂盒,快速确定蛋白质的含量,然后用SDS/PAGE分析蛋白质的分布。
11) 目标蛋白质需要进一步纯化需要根据蛋白质的用途确定。
12) 纯化的目标蛋白质需要复性,复性常用的手段可以参考有关手册确定的原则。
GuNTA-0 、20、40、60、100、500Buffer分别为浓度20 mM Tris-HCl pH7.9, 0.5 M NaCl, 10% Glycerol,6 M Guanidium HCl添加0、20、40、60、100、500 mM Imidazole。
C. NTA树脂的再生
NTA树脂在使用若干次数(3-5次)后,结合效率有所下降,可以用以下方法再生,提高树脂的使用寿命和蛋白质的结合效率。
NTA树脂再生前需要从层析柱下端流干所有溶液,估计出NTA的树脂体积,按下列次序将再生试剂加到层析柱里,在等上一步再生溶液流干后,再加下一步再生溶解。
用户需要自行准备25%、50%、75%、100%(v/v)乙醇和去离子水。 从层析柱下端流干所有溶液,用2倍NTA树脂体积的Stripping Solution I、2倍体积的去离子水、3倍体积的Stripping Solution II、1倍体积的25%乙醇、1倍体积的50%乙醇、1倍体积的75%乙醇、5倍体积的100%乙醇、1倍体积的75%乙醇、1倍体积的50%乙醇、1倍体积的25%乙醇、1倍体积的去离子水、5倍体积的Stripping Solution III、3倍体积的去离子水分别洗一遍。
如果立即使用,用5倍体积的Ni Charging Solution洗,再用10倍体积的平衡溶液(NTA-0Buffer或GuNTA-0 Buffer)洗;如果想长期储存,加入1倍体积的20%乙醇,4°C保存,使用前用5倍体积的Ni Charging Solution洗,再用10倍体积的平衡溶液(NTA-0Buffer或GuNTA-0 Buffer)洗
再生溶液配方:Stripping Solution I: 6M GuHCl, 0.2M acetic acid。Stripping Solution II: 2% SDS。 Stripping Solution III: 100 mM EDTA, pH 8.0。Ni Charging Solution: 100 mM NiSO4
备注:产品信息可能会有优化升级。请以实际标签信息为准。
DEAE Sepharose 6FF的重力柱
| 规格 | 1x1mL 5x1mL 1x5mL 5x5mL |
CM Sepharose 6FF的重力柱
| 规格 | 1x1mL 5x1mL 1x5mL 5x5mL |
是一种弱阳离子交换树脂,适用于实验室规模和工业规模的蛋白质纯化制备。
Octyl-Sepharose 4FF的重力柱
| 规格 | 1x1mL 5x1mL 1x5mL 5x5mL |
Octyl Beads 4FF:属于脂肪族疏水作用介质,由90微米高度交联的琼脂糖组成,配基通过不带电和化学性质十分稳定的醚键连接到琼脂糖上。
环氧活化-琼脂糖凝胶4FF
| 有效期 | 1年 |
| 英文名称 | Epoxy activated Sepharose 4FF |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 25ml |
说明:分离试剂
产品介绍:
Epoxy- Activated Beads 4FF 是一种环氧活化的琼脂糖微球,可以直接用于含氨基、巯基和羟基的蛋白和样品的耦联。预活化介质可以根据需要制备成特殊的亲和介质,快速有效地从复杂体系中一步纯化相应的物质。
Epoxy- Activated Beads 4FF 产品性能:
|
性能 |
指标 |
|
基质 |
高度交联的 4%琼脂糖微球 |
|
活性基团密度 |
30-40μmol/ml 介质 |
|
粒 径 (μm) |
45-165 |
|
最大压力 |
0.3 MPa, 3bar |
|
储存缓冲液 |
100% 1,4-二氧六环 |
|
储存温度 |
室温 |
操作说明:
1、 溶液的准备
偶联液:0.1M Na2CO3, pH8.5-10.0
封闭液:1M 乙醇胺,pH8.0
清洗液1:0.1M 乙酸–乙酸钠,0.5M NaCl,pH4.0
清洗液2:0.1M Tris-HCl,0.5M NaCl,pH8.0
保存液: 含20%乙醇的1XPBS
2、 样品准备
样品用偶联液溶解,浓度约5-10mg/ml。
3、 样品偶联
a、取适量的 Epoxy-Activated Beads 4FF,去除保护液,切勿抽干,去离子水清洗三次, 用偶联液清洗一次。
b、将溶解好的样品中溶解后转入清洗好的 Epoxy-Activated Beads 4FF 中,填料:样品溶液体积比约为 1: 1-2。
c、25-40℃振荡混合反应 24h。注:确保树脂悬浮起来,否则会大大影响偶联效率。
反应完后收集偶联样品,以便检测偶联效率。偶联液清洗一遍。
d、加入等体积的封闭液,37 度振荡混合反应 1h。
e、将上述反应体系取出,流干其中的溶液,用 3 倍柱体积的去离子水清洗树脂,清洗液 1、去离子水、清洗液 2 和去离子水重复冲洗 2 次,然后保存在等体积的保护液中,于 2℃-8℃保存。
备注:产品信息可能会有优化升级。请以实际标签信息为准。
丁基-琼脂糖凝胶4FF
| 有效期 | 2年 |
| 英文名称 | Butyl-Sepharose 4FF |
| 储存条件 | 2-8℃ |
| 外观(性状) | 颗粒 |
| 单位 | 瓶 |
| 规格 | 25ml |
丁基-琼脂糖凝胶 4FF是将丁基键合在琼脂糖凝胶4FF上形成的一种可利用疏水相互作用来实现目标产品纯化分离的疏水类介质。用于生物大分子和乙肝疫苗的纯化分离。
1 外观
本品为白色球状凝胶,无嗅、无味、无肉眼可见杂质。
2 理化指标
|
项 目 |
指 标 |
|
配基 |
丁基 |
|
基质 |
4% 交联琼脂糖凝胶 |
|
形状 |
球形 |
|
粒径 |
45~165 μm |
|
配基密度 |
40 μmol/ml介质 |
|
最高流速(25℃) |
100KPa下200 cm/h* |
|
耐压 |
0.2 MPa |
|
工作温度 |
4~40℃ |
|
pH适用范围 |
2~14(短时间 ,在位清洗);3~13(长时间) |
|
化学稳定性 |
以下溶液中稳定: pH3~12.5中稳定;0.1% triton水溶液和1%MOPS溶液中稳定;5%甲醛中基本稳定 |
*柱子:内径16mm、柱长10cm,柱床高5cm,25℃,流动相为0.1mol/LNaCl。
3 包装
产品以无菌试剂瓶密封包装,外贴标签,注明“品名、体积、颗粒大小、应用、生产单位”等内容。所选用的包装应有利于保证产品质量、方便运输和贮存。
4 运输
运输中应避免日晒、雨淋、重压,严禁与有毒、有害物品混运。
5 贮存
产品应密封贮存在4℃~30℃(保存溶液为20% 乙醇+0.1M醋酸钠),通风、干燥、清洁的地方。不能冷冻。
用过的柱子贮存在4℃(20% 乙醇)。
6 保质期:
5年。
7 应用
丁基-琼脂糖凝胶 4FF是一种疏水层析介质,利用样品中组分疏水性的不同进行分离。用于生物大分子的纯化分离。
下面简要介绍介质的使用过程。
7.1 装柱
(1)让所有的材料和试剂达到室温。配制初始缓冲液(平衡液)和洗脱缓冲液。
(2)根据柱子大小取所需量的凝胶,清洗掉20%乙醇,抽干,用初始缓冲液(按凝胶:缓冲液=3:1的比例)配成匀浆。
(3)将柱内及柱子底端用水或缓冲液润湿并保持一小段液位(液面略高于滤膜),务必使底端无气泡。
(4)用玻璃棒引导匀浆沿着柱内壁一次性倒入柱内,注意勿使产生气泡。打开柱子出液口,使凝胶在柱内自由沉降,连结好柱子顶端柱头。
(5)打开蠕动泵,让缓冲液用使用时流速的1.33倍的流速流过,使柱床稳定。用2~3倍柱体积的缓冲液平衡柱子。
7.2 平衡
让平衡缓冲液以一定流速流过柱子,到流出液电导和pH不变。平衡缓冲液一般是高盐浓度的缓冲液,如0.02~0.05mol/L的PBS加1~2.5mol/L(NH4)2SO4等。
7.3 上样
(1)样品用平衡液配制,浑浊的样品要离心和过滤后上样。
(2)一般情况是让目标产品结合在柱子上,用平衡液洗去杂质,再选择一种洗脱液洗下目标产品。
(3)介质对样品组分吸附的程度取决于样品的疏水性质、流动相的离子强度和温度。盐浓度大、温度高或样品组分疏水性强,介质对组分吸附牢。
7.4 洗脱
疏水介质可用减小盐浓度进行洗脱。加表面活性剂或有机溶剂可加强洗脱。最常用的洗脱液是低盐浓度缓冲液,如0.02~0.05mol/L的PBS。
7.5 再生
一般用低盐浓度的缓冲液洗,洗10倍以上柱体积,接着用结合蛋白的平衡液洗到平衡,可再次使用。
若有失活蛋白质或脂类物质在再生时洗不掉,可用在位清洗(CIP)除去。
7.6 在位清洗
(1)对于以离子键结合上去的蛋白,可以用2M Nacl去除。
(2)对沉淀蛋白、对以疏水性结合的蛋白或脂类,可用1M NaOH 去除。
(3)对强疏水性结合的蛋白、脂类等,用4~10倍柱体积的70%乙醇或30%异丙醇清洗,但要注意有机溶剂的浓度以梯度的方式逐渐增加,否则容易产生气泡。
清洗完毕后,用至少3倍缓冲液平衡柱子。
7.7 注意
在装柱、使用和保存柱子的时候,要避免柱子流干,气泡进入。
7.8 去热源
用0.5M的氢氧化钠清洗柱子5~6小时或用0.1M的氢氧化钠24小时。或用以下方法步骤去除:
(1)2倍柱体积的70%乙醇;
(2)2倍柱体积50mM Tris-Hcl pH7.5;
(3)1倍柱体积4M尿素;
(4)3倍柱体积的Tris缓冲液+0.1M Nacl;
上缓冲液都在无热源的双蒸水中配制。
7.9 消毒 用0.5~1M NaOH室温下洗8~10倍柱体积,初始缓冲液平衡柱子。
特别注意:
上样之前,样品必须去除色素,否则色素会被吸附到填料上,影响填料的正常使用。
备注:产品信息可能会有优化升级。请以实际标签信息为准。
红色-琼脂糖凝胶6FF
| 有效期 | 1年 |
| 英文名称 | Red Sepharose 6FF |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 25ml 100ml |