| MDL |
MFCD00077757 |
| EC |
EINECS 246-818-3 |
| 别名 |
羟基柔红霉素盐酸盐; ADM hydrochloride; DOX HCl |
| 英文名称 |
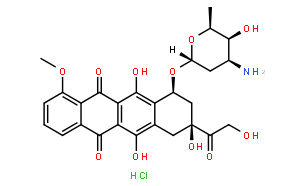
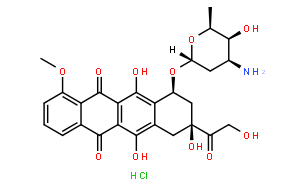
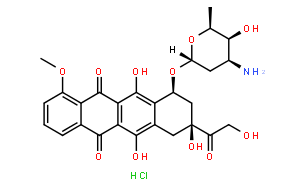
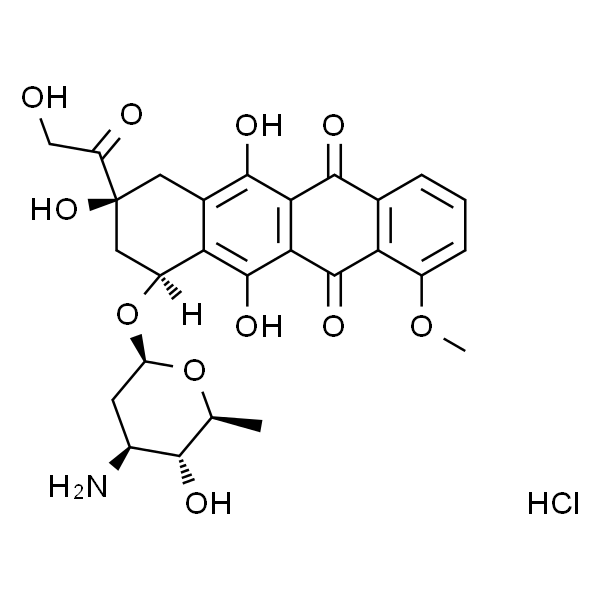
Doxorubicin Hydrochloride |
| CAS |
25316-40-9 |
| 分子式 |
C27H29NO11·HCl |
| 分子量 |
579.99 |
| 纯度 |
HPLC≥98% |
| 单位 |
瓶 |
| 生物活性 |
Doxorubicin hydrochloride是一种有细胞毒性的蒽环类抗生素。 Doxorubicin 在癌细胞中起作用的可能机制是嵌入 DNA 和破坏 topoisomerase-II 介导的DNA修复。[1-4] |
| In Vitro |
在最高测试浓度 (分别为2μM和10μM) 下阿霉素和辛伐他汀的组合可杀死97%的Hela细胞[2]。 |
| In Vivo |
携带PC3异种移植物的小鼠注射2, 4或8mg / kg多柔比星, 并随时间测量肿瘤体积。 2mg / kg的剂量不影响肿瘤生长, 而较高剂量最初延迟肿瘤生长 (第18天和第22天p <0.05) , 4mg / kg或8mg / kg阿霉素显着降低PC3异种移植物中c-FLIP的水平。 [3]。单次腹膜内注射10mg / kg (多柔比星1) 在大鼠中给药, 每天10次腹膜内注射1mg / kg (多柔比星2) , 或每周5次腹膜内注射2mg / kg (多柔比星3) 。在阿霉素1中第28天观察到80%的死亡率, 而在第107天和第98天, 阿霉素2和阿霉素3分别达到80%的死亡率。在多柔比星DOX1中, 第2周的分数缩短减少30%, 在阿霉素2中第13周减少55%, 在阿霉素3中第13周减少42%[4]。 |
| SMILES |
COC1=C2C(C(C(C(O)=C(C[C@](C(CO)=O)(O)C[C@@H]3O[C@@]4([H])C[C@H](N)[C@H](O)[C@H](C)O4)C3=C5O)=C5C2=O)=O)=CC=C1.[H]Cl |
| 靶点 |
Topoisomerase |
| 动物实验 |
小鼠[3]使用无胸腺雄性裸鼠 (3-4周龄) 。将PC3细胞 (4×106) 皮下注射到小鼠的侧腹中。将携带肿瘤的动物随机分配到治疗组 (每组5或6只小鼠) , 并且当异种移植物达到约100mm 3的体积时开始治疗。使用数字卡尺测量肿瘤并使用以下公式计算体积:体积=宽度2×长度×0.52, 其中宽度表示肿瘤的较短尺寸。如所示使用载体 (含有0.1%BSA的PBS) , 阿霉素 (2-8mg / kg) , Apo2L / TRAIL (500μg/动物) 或4mg / kg多柔比星的组合然后500μgApo2L/的施用来施用处理。落后。全身施用阿霉素, 而在肿瘤内或全身施用Apo2L / TRAIL。所有治疗都给予一次。每天监测小鼠的不良反应迹象 (无精打采和邋app的外观) 。治疗似乎很好耐受。计算每个数据点的平均值±SEM。通过学生t检验分析治疗组之间的差异。当P <0.05时, 差异被认为是显着的。大鼠[4]将30只雄性Sprague-Dawley大鼠 (体重250-300g) 随机分配到3个实验组中的1个:阿霉素方案1 (多柔比星1, n = 10) , 阿霉素方案2 (多柔比星2, n = 10) , 或阿霉素方案3 (多柔比星3, n = 10) 。对于所有阿霉素治疗方案, 阿霉素的累积剂量为10mg / kg。附表1涉及以10mg / kg单次推注腹膜内注射阿霉素。附表2涉及以1mg / kg连续10天腹膜内注射多柔比星10次。附表3涉及5次腹膜内注射2mg / kg的阿霉素, 每周一次, 持续5周。在第一次阿霉素治疗之前和开始阿霉素治疗后每周一次, 在所有存活的动物中评估血压和心脏功能, 只要每组至少有3只大鼠。 |
| 细胞实验 |
将160μLHela细胞悬浮液 (3×10 4细胞/ mL) 分配到三个96孔U形底微量培养板中, 并在37℃, 5%CO 2的完全湿润气氛中孵育24小时。在板1中, 加入多柔比星 (20μL; 终浓度, 0.1-2μM) 和辛伐他汀 (20μL; 终浓度, 0.25-2μM) 的连续稀释液至终体积200μL并再孵育72小时。在板2和3中, 加入每种药物 (辛伐他汀或多柔比星, 40μL) 的连续稀释液。在24小时的温育期后, 吸出培养基并在PBS中洗涤细胞。然后, 加入其他药物 (40μL) 的连续稀释液并补充培养基至终体积为200μL, 并孵育48小时。多柔比星和辛伐他汀单独用作阳性对照 (每孔40μL) , 仅用溶剂处理的细胞被认为是阴性对照。为了评估细胞存活, 向每个孔中加入20μLMTT溶液 (PBS中5mg / mL) 并孵育3小时。然后用150μLDMSO代替培养基, 并通过重复移液溶液实现甲crystals晶体的完全溶解。然后通过ELISA板读数器在540nm测定吸光度。在4或8个孔中测定每种药物浓度并重复3次。阿霉素的细胞毒性/细胞抑制作用表示为相对存活率 (%对照) 并计算。阴性对照中细胞存活的百分比假定为100.相对存活率= (实验吸光度 – 背景吸光度) / (未处理对照的吸光度 – 背景吸光度) ×100%[2]。 |
| 数据来源文献 |
[1]. Nitiss JL, et al. Targeting DNA topoisomerase II in cancer chemotherapy.Nat Rev Cancer. 2009 May; 9 (5) :338-50.[2]. Sadeghi-Aliabadi H, et al. Cytotoxic evaluation of doxorubicin in combination with simvastatin against human cancer cells. Res Pharm Sci. 2010 Jul; 5 (2) :127-33.[3]. El-Zawahry A, et al. Doxorubicin increases the effectiveness of Apo2L/TRAIL for tumor growth inhibition of prostate cancerxenografts. BMC Cancer. 2005 Jan 7; 5:2.[4]. Hayward R, et al. Doxorubicin cardiotoxicity in the rat: an in vivo characterization. J Am Assoc Lab Anim Sci. 2007 Jul; 46 (4) :20-32 |
| 备注 |
以上数据均来自公开文献, Jinpan暂未进行独立验证, 仅供参考。These protocols are for reference only. Jinpan does not independently validate these methods. |
| 规格 |
10mg 10mM*1mL (in DMSO) 50mg |