甘草次酸(β型) 标准品
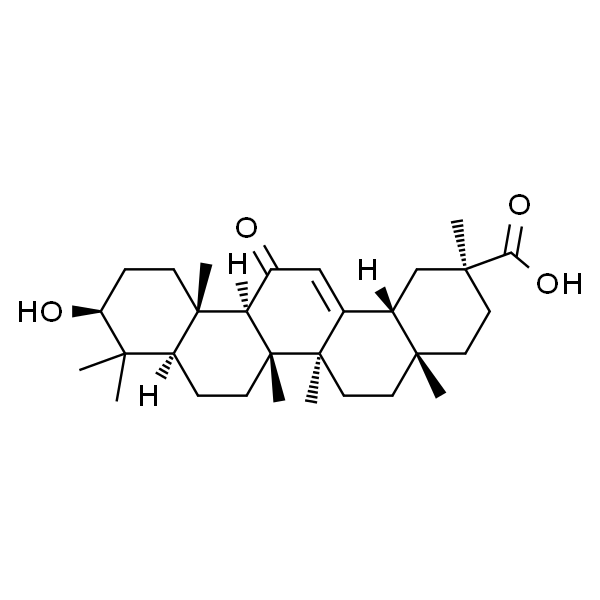
| 别名 | 18β-甘草次酸;(3β,18β)-3-羟基-11-氧代-齐墩果-12-烯-29-酸 |
| 英文名称 | Clycyrrhetinic Acid |
| CAS | 471-53-4 |
| 分子式 | C30H46O4 |
| 分子量 | 470.68 |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 20mg |

甘草次酸(β型) 标准品

| 别名 | 18β-甘草次酸;(3β,18β)-3-羟基-11-氧代-齐墩果-12-烯-29-酸 |
| 英文名称 | Clycyrrhetinic Acid |
| CAS | 471-53-4 |
| 分子式 | C30H46O4 |
| 分子量 | 470.68 |
| 储存条件 | 2-8℃ |
| 单位 | 瓶 |
| 规格 | 20mg |
Enoxolone;18β-甘草次酸
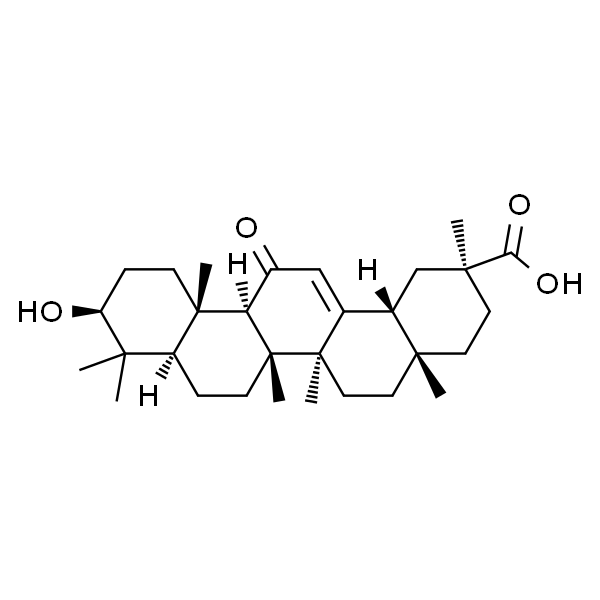
| MDL | MFCD00003706 |
| EC | EINECS 207-444-6 |
| InChIKey | MPDGHEJMBKOTSU-YKLVYJNSSA-N |
| InChI | InChI=1S/C30H46O4/c1-25(2)21-8-11-30(7)23(28(21,5)10-9-22(25)32)20(31)16-18-19-17-27(4,24(33)34)13-12-26(19,3)14-15-29(18,30)6/h16,19,21-23,32H,8-15,17H2,1-7H3,(H,33,34)/t19-,21-,22-,23+,26+,27-,28-,29+,30+/m0/s1 |
| PubChem CID | 10114 |
| 别名 | 18β-GlycyrrhetinicAcid;Glycyrrhetinate |
| 英文名称 | Enoxolone |
| CAS | 471-53-4 |
| 分子式 | C30H46O4 |
| 分子量 | 470.68 |
| 纯度 | HPLC≥98% |
| 单位 | 瓶 |
| 生物活性 | Enoxolone是甘草的主要生物活性成分,具有抗溃疡,抗炎和抗增殖的特性。[1-3] |
| In Vitro | 18β-甘草次酸是甘草的主要生物活性成分, 具有抗溃疡, 抗炎和抗增殖的特性。 MTS测定表明, 18β-甘草次酸的24小时处理以剂量依赖性方式抑制两种细胞系中的细胞增殖。在160μM的18β-甘草次酸显着降低活细胞百分比至A549的约40.5±10.5%和NCI-H460的38.3±4.6% (分别为p <0.01) 。当用320μM18β-甘草次酸处理细胞时, 显示出对细胞增殖的更大抑制作用, 因为与未处理的对照相比, 活细胞的百分比低于30% (p <0.001) 。用180μM和320μM的18β-甘草次酸处理降低了全长PARP的水平并增加了切割的PARP水平[1]。 |
| In Vivo | 与TP大鼠相比, 接受低剂量18β-甘草次酸 (50mg / kg) 的18β-甘草次酸+雷公藤内酯醇 (TP) 组大鼠的三种血清参数均显着降低。 18β-甘草次酸+ TP组大鼠接受高剂量18β-甘草次酸 (100mg / kg) 后, 三种肝酶水平略有降低, 与TP组比较, 降低程度无统计学意义。相比之下, 预先给予低剂量18β-甘草次酸可以保护动物免受TP诱导的肝脏病变。相反, 低剂量的18β-甘草次酸 (50mg / kg) 显着抑制了上述四种细胞因子的释放[3]。 |
| SMILES | CC1(C)[C@@H](O)CC[C@]([C@@]1([H])CC[C@@]([C@@]2(CC[C@]3(CC[C@](C(O)=O)(C[C@]3(C2=C4)[H])C)C)C)5C)(C)[C@@]5([H])C4=O |
| 靶点 | Dehydrogenase inhibitor |
| 动物实验 | 使用健康Wistar大鼠 (雄性, 200±20g) 并将其分成5组, 每组随机10个个体。正常对照 (NC) 组中的动物在最后3天接受蒸馏水6天和0.5%CMC-Na。雷公藤内酯模型组 (TP) , 18β-甘草次酸低剂量组 (GAL + TP) 和18β-甘草次酸高剂量组 (GAH + TP) 的大鼠接受蒸馏水, 18β-甘草次酸 (50mg / kg) , po, 溶于蒸馏水) , 或18β-甘草次酸 (100 mg / kg, po, 溶于蒸馏水) , 分别连续6天, TP引起肝损伤 (2.4 mg / kg, po, 暂停最后3天, 在0.5%CMC-Na中) 。在过去3天后, 上述三组动物在蒸馏水或18β-甘草次酸处理后6小时接受TP [3]。 |
| 细胞实验 | 在该研究中使用原代小胶质细胞培养物。对于治疗分析, 将小胶质细胞与完全DMEM一起孵育, 并在存在或不存在18β-甘草次酸 (25μM和50μM) 的条件下, 在37℃, 5%湿润培养箱中, 使用或不使用100 ng / mL IFN-γ进行刺激。 CO2。对于细胞迁移试验, 用或不用IFN-γ (100ng / mL) 刺激接种于完全DMEM培养基中的分离的原代小胶质细胞, 并用不同剂量的18β-甘草次酸处理, 24小时后, 小胶质细胞培养上清液为收集并添加到Transwell插入物的下室[2]。 |
| 数据来源文献 | [1]. Huang RY, et al. 18β-Glycyrrhetinic acid suppresses cell proliferation through inhibiting thromboxane synthase in non-small cell lung cancer. PLoS One. 2014 Apr 2; 9 (4) :e93690.
[2]. Zhou J, et al. 18β-glycyrrhetinic acid suppresses experimental autoimmune encephalomyelitis through inhibition of microglia activation and promotion of remyelination. Sci Rep. 2015 Sep 2; 5:13713. [3]. Yang G, et al. Protective Effect of 18β-Glycyrrhetinic Acid against Triptolide-Induced Hepatotoxicity in Rats. Evid Based Complement Alternat Med. 2017; 2017:3470320. |
| 备注 | 以上数据均来自公开文献, Jinpan暂未进行独立验证, 仅供参考。These protocols are for reference only. Jinpan does not independently validate these methods. |
| 规格 | 50mg 10mM*1mL in DMSO 100mg 500mg |
是甘草的主要生物活性成分,具有抗溃疡,抗炎和抗增殖的活性。
乙酰甘草次酸
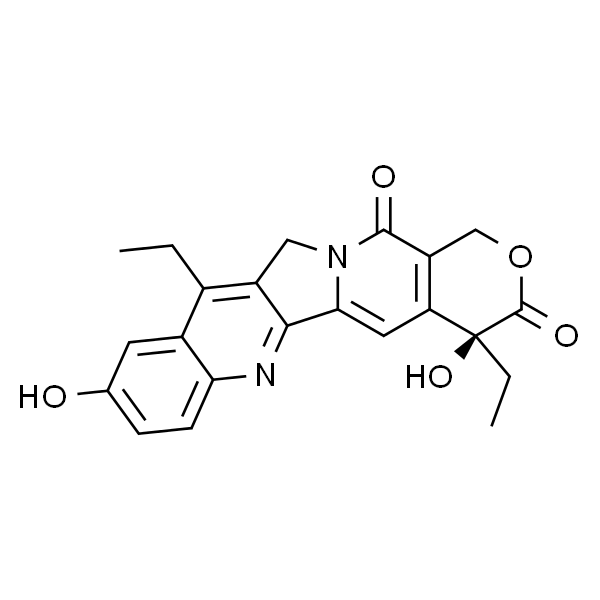
| MDL | MFCD06762720 |
| EC | EINECS 643-093-9 |
| 别名 | 7-乙基-10-羟基喜树碱; EHCPT |
| 英文名称 | SN-38 |
| CAS | 86639-52-3 |
| 分子式 | C22H20N2O5 |
| 分子量 | 392.4 |
| 储存条件 | 2~8度 |
| 纯度 | Purity≥98% |
| 单位 | 瓶 |
| 生物活性 | SN-38是拓扑异构酶I抑制剂伊立替康的活性代谢产物。 SN-38抑制DNA合成和RNA 合成的IC50分别为0.077 和 1.3 μM。[1-3] |
| In Vitro | LoVo,HCT116和HT29细胞系的IC 50值分别为20nM,50nM,130nM。在所有三种SN-38抗性细胞系中,Top1活性在高浓度SN-38存在下维持[2]。 |
| In Vivo | SN-38,抗癌前药伊立替康的活性和毒性代谢产物。在给药后30分钟,Slco1a/1b( -/- )小鼠中的伊立替康血浆浓度比野生型小鼠高1.9倍(分别为1.89对1.01μM),而SN-38血浆浓度为Slco1a /与野生型小鼠相比,1b( -/- )小鼠高8倍(分别为0.4μg/ mL对0.05μg/ mL)。伊立替康的总体血浆暴露[AUC(5-240)]在Oatp1a/1b敲除小鼠中比野生型小鼠高1.7倍(209.8±6.7对比120.9±4.4μM/ min; P <0.01),并且2.9- SN-38折叠率更高(50±2.9对12±2μM/ min; P <0.001)[3]。 |
| 激酶实验 | 将LoVo,HCT116和HT29细胞系用胰蛋白酶处理,重新悬浮并计数,并且对于每个细胞系,将100万个细胞移液到冰上的三个eppendorf管中的每一个上。将细胞沉淀(离心5分钟,300g,4℃)并在干冰和乙醇中快速冷冻并储存在-80℃直至分析。基本上制备核提取物,并且使用标准滚环增强酶活性检测(REEAD)方案,在添加或不添加SN-38(在文中所述的浓度)的滴定实验中测量Top1活性。根据Top1特定信号的数量计算活性,该信号相对于添加已知浓度的对照圆所产生的信号量[2]。 |
| SMILES | O=C1[C@](O)(CC)C2=C(CO1)C(N3CC4=C(CC)C5=CC(O)=CC=C5N=C4C3=C2)=O |
| 靶点 | Topoisomerase |
| 动物实验 | 小鼠[3]雌性野生型,Slco1a/1b( – / – )(Oatp1a/1b敲除),Slco1a/1b( – / – ); 1B1(tg)和Slco1a/1b( – / – ); 1B3(使用具有相当的遗传背景(> 99%FVB)的8至14周龄的(肝特异性OATP1B1和OATP1B3人源化转基因)小鼠。伊立替康(20mg/mL,在含有NaOH,乳酸和山梨糖醇的水基溶液中)用盐水(至2mg/mL)稀释,给药10mg/kg;向小鼠静脉内施用5μL/ g体重。将SN-38溶解于DMSO(1mg/mL)中,并向小鼠静脉内施用1μL/ g体重,以达到1mg/kg的剂量。通过异氟醚麻醉,通过心脏穿刺进行肝素 – 血液取样,然后进行颈椎脱位和组织收集来终止实验。将血液样品以5,200×g在4℃下离心5分钟,收集血浆并储存在-30℃直至分析。 |
| 细胞实验 | 使用MTT测定法测定体外SN-38敏感性。将细胞接种在96孔板中,第二天加入一系列SN-38浓度。在药物暴露48小时后,弃去培养基并将板与含有MTT(0.5mg/mL)的培养基一起温育3小时。加入酸化的(0.02M HCl)十二烷基硫酸钠(20%)以溶解形成的甲..测量570nm处的光密度(和背景的670nm),并且与未处理的细胞相比以百分比计算细胞存活率。实验重复三次,测定平均IC50值±标准偏差。通过将抗性细胞系的平均IC 50值除以相应亲本细胞系的平均IC 50值来计算每种抗性细胞系的相对抗性[2]。 |
| 数据来源文献 | [1]. Wallin A, et al. Anticancer effect of SN-38 on colon cancer cell lines with different metastatic potential. Oncol Rep. 2008 Jun;19(6):1493-8. [2]. Jensen NF, et al. Characterization of DNA topoisomerase I in three SN-38 resistant human colon cancer cell lines reveals a newpair of resistance-associated mutations. J Exp Clin Cancer Res. 2016 Mar 31;35:56. [3]. Stewart CF, et al. Disposition of irinotecan and SN-38 following oral and intravenous irinotecan dosing in mice. Cancer Chemother Pharmacol. 1997;40(3):259-65 |
| 规格 | 20mg 50mg 100mg |
SN-38可以抑制DNA topoisomerase I,DNA合成,并造成频繁的DNA单链断裂。
诃子次酸 标准品

| 保存 | 2-8°C |
| 有效期 | 2 years |
| 英文名称 | Chebulic Acid |
| CAS | 23725-05-5 |
| 分子式 | C14H12O11 |
| 分子量 | 356.24 |
| 纯度 | HPLC≥98% |
| 外观(性状) | Solid |
| 单位 | 瓶 |
| 规格 | 5mg |
β-甘草次酸 标准品
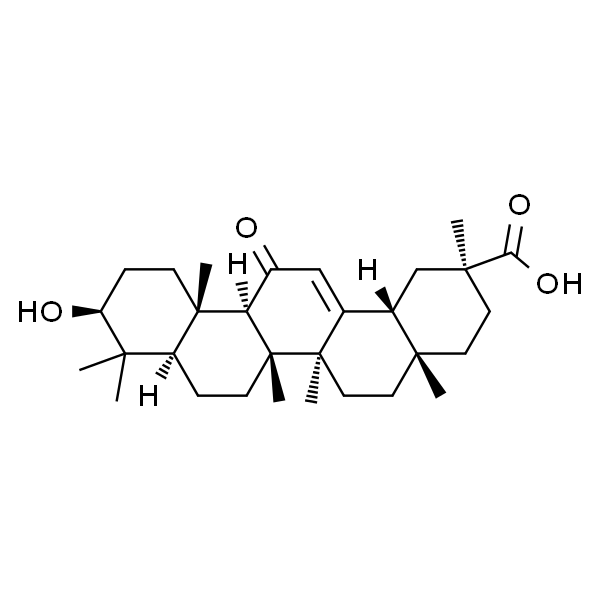
| EC | EINECS 207-444-6 |
| MDL | MFCD00003706 |
| 别名 | 甘草亭酸 |
| 英文名称 | Enoxolone |
| CAS | 471-53-4 |
| 分子式 | C30H46O4 |
| 分子量 | 470.68 |
| 储存条件 | 2-8℃ |
| 纯度 | HPLC≥98% |
| 外观(性状) | Off-white Powder |
| 单位 | 瓶 |
| SMILES | CC1(C)[C@@H](O)CC[C@]([C@@]1([H])CC[C@@]([C@@]2(CC[C@]3(CC[C@](C(O)=O)(C[C@]3(C2=C4)[H])C)C)C)5C)(C)[C@@]5([H])C4=O |
| 规格 | 20mg |